Понимание слабых электролитов по Аррениусу: теория и практика
Теория слабых электролитов Аррениуса объясняет поведение электролитов в растворах и их влияние на проводимость. Эта теория имеет ключевое значение для химии и биохимии, так как помогает понять процессы ионного обмена, электролитические свойства веществ и многое другое. В этом разделе вы найдете подборку фотографий и полезных советов, которые помогут углубить ваше понимание этой теории и ее практических приложений.



Изучайте примеры слабых электролитов, таких как уксусная кислота и аммиак, чтобы лучше понять теорию Аррениуса.

Теории кислот, оснований и растворов. Теория Аррениуса-Оствальда. 11 класс.

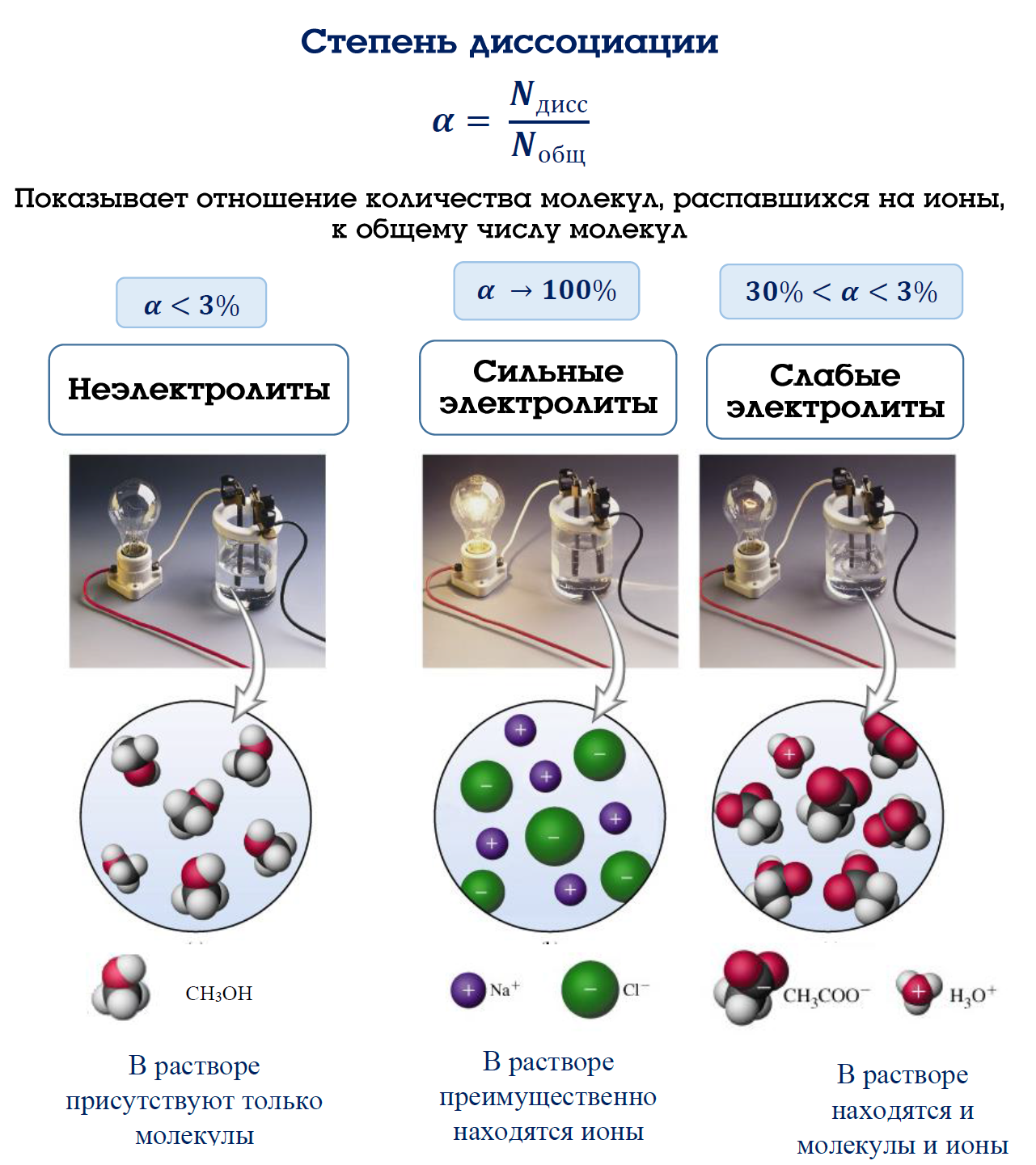
Обратите внимание на степень диссоциации слабых электролитов, которая обычно низка и зависит от концентрации раствора.

Физическая химия 2 (Электрохимия) — Лекция 1 — Введение, теория Аррениуса

Используйте проводимость растворов для определения силы электролитов, так как слабые электролиты проводят электричество хуже сильных.

Квантовая электродинамика. Теория всего-не законченная теория Эйнштейна.

Экспериментируйте с разбавлением растворов слабых электролитов и наблюдайте за изменениями в их свойствах.

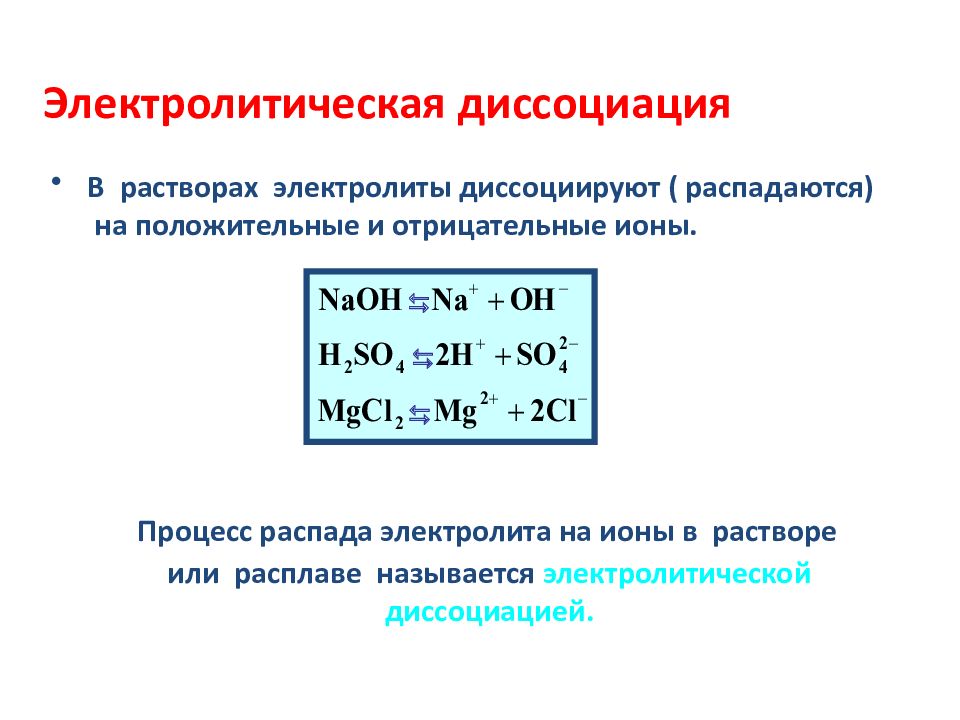
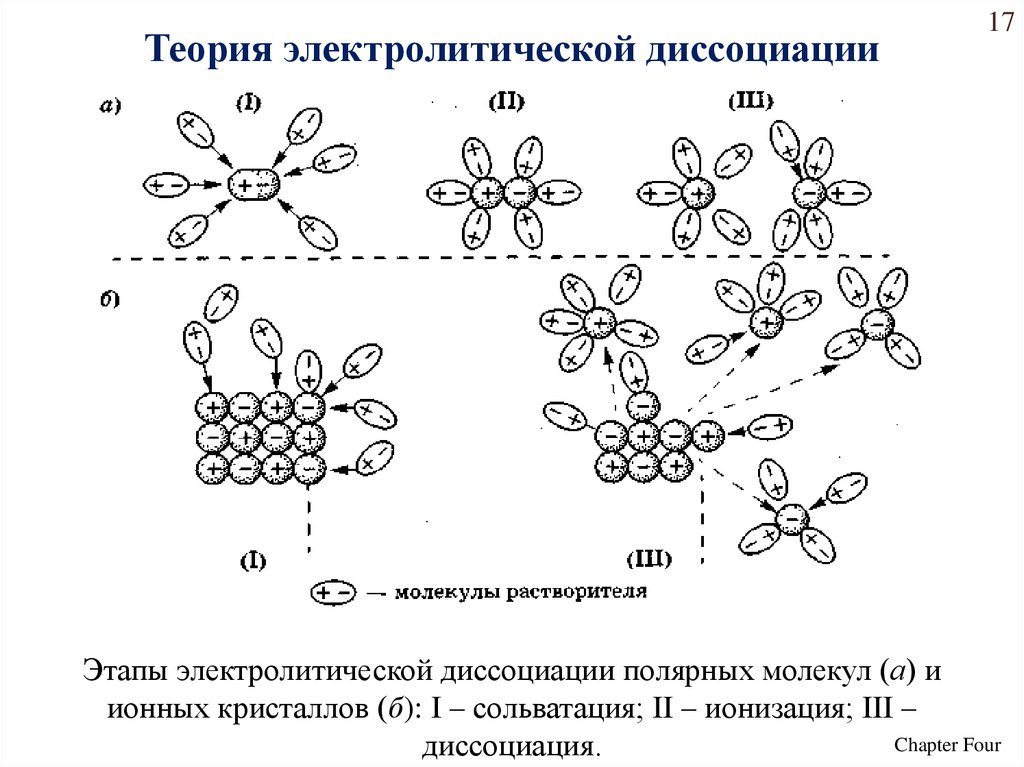
Теория электролитической диссоциации
Изучите влияние температуры на степень диссоциации слабых электролитов.

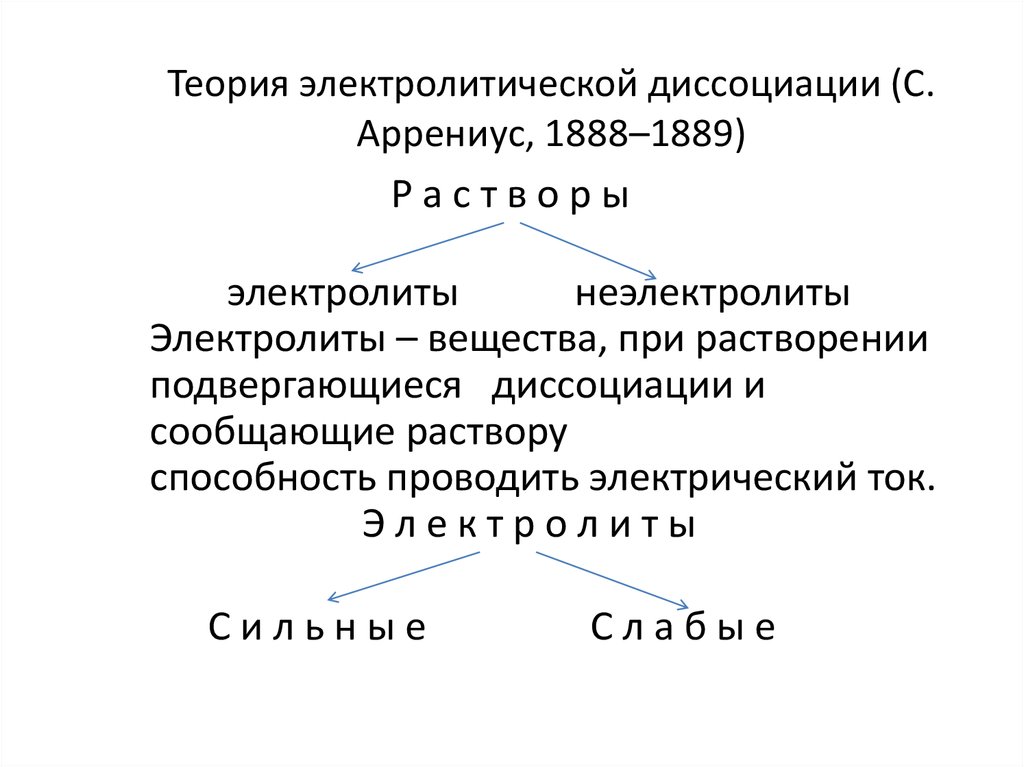
Основные положения теории электролитической диссоциации - Химия 8 класс #41 - Инфоурок
Применяйте теорию Аррениуса для объяснения кислотно-основных свойств растворов.

ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ХИМИЯ 8 класс // Подготовка к ЕГЭ по Химии - INTENSIV

Ищите практические приложения теории слабых электролитов в биохимии и медицине.

Используйте PH-метрию для оценки кислотности растворов слабых электролитов.

Степень электролитической диссоциации. Сильные и слабые электролиты. 9 класс.
Изучайте историческое развитие теории Аррениуса и её вклад в современную химию.

Лекция 41 Описание электропроводности слабых электролитов


Обращайте внимание на различия между сильными и слабыми электролитами в учебных материалах и лабораторных работах.

сильные и слабые электролиты РАСЧЕТ рН